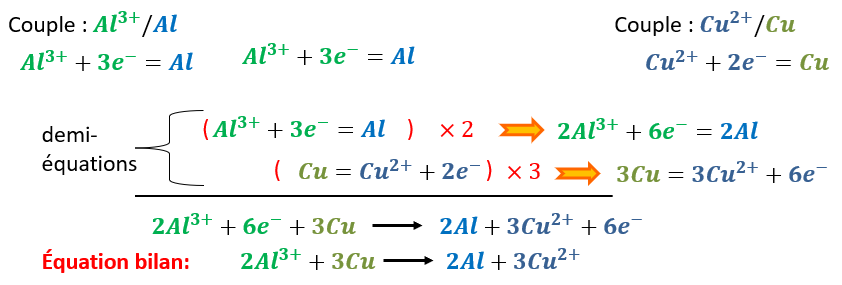Oxydoréduction
Un Oxydant est espèce chimique susceptible de capter (Obtenir) un ou plusieurs électrons.
Un Réducteur est une espèce chimique susceptible de céder (Rendre) un ou plusieurs électrons.
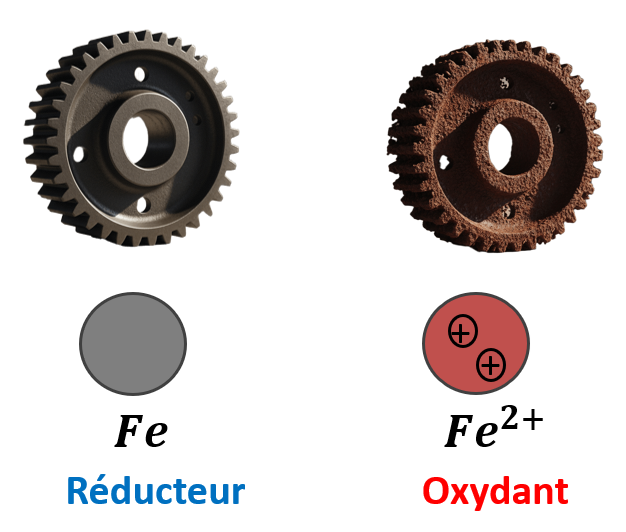
Un oxydant est toujours associé à un réducteur.
Ils forment ensemble un couple oxydant/réducteur, aussi apppellé couple REDOX.
Pour noter un couple redox, on commence toujours par l’oxydant:

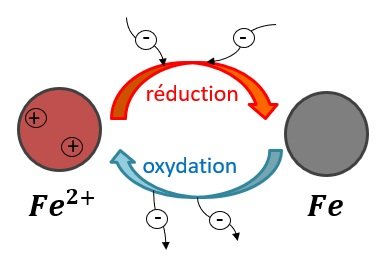
Chaque couple redox posède une demi-équation électronique qui décrit la transformation de l’oxydant en réducteur ou inversement.
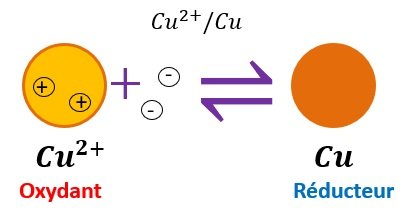
Une demi-équation électronique pôuvant s’effectuer dans les deux sens, il faut utiliser un signe égal ou une double flêche entre l’oxydant et les électrons à droite, et le réducteur à gauche.
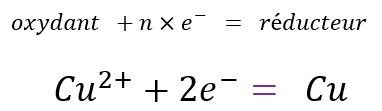
Pour certaines demi-équations il ne suffit pas de mettre le bon nombre d’électrons aux côtés de l’oxydant, il faut ajouter des molécules d’eau et des ions hydrogènes.
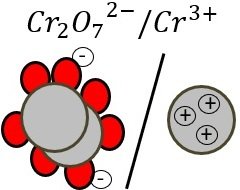
En milieu acide (classe de 1SPE), il suffit de respecter 4 étapes pour équilbrer une demi-équation :

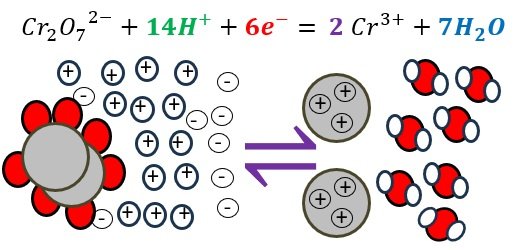
Transformation d'oxydoréduction
Lors d’une transformation d’oxydoréduction, il y a toujours deux couples redox impliqués, l’oxydant du premier couple réagissant avec le réducteur du second couple.
La réaction formera alors le réducteur du premier couple ainsi que l’oxydant du second couple.
Exemple:
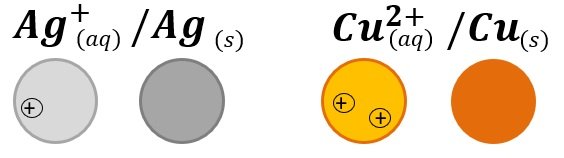
La transformation de
est issue de la réaction entre les ions argents contenus dans la solution de nitrate d’argent et le cuivre métallique.
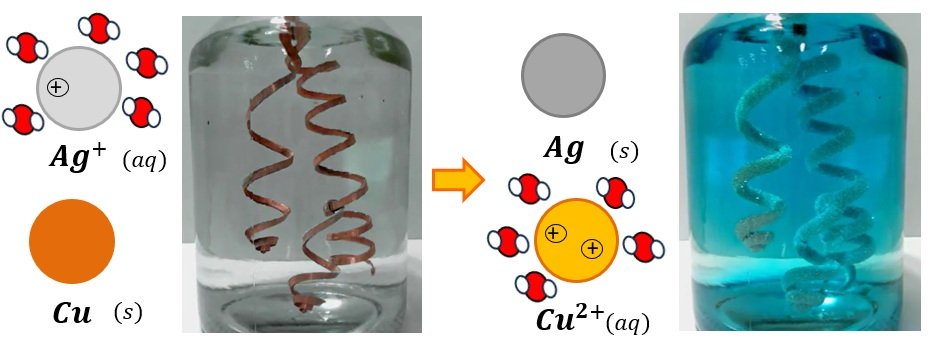
Cette transformation produit de l’argent métallique et des ions cuivre II qui vont donner une teinte bleutée à la solution.
L’équation bilan de cette transformation d’oxydoréduction s’écrit :
Pour écrire l’équation bilan d’une transformation d’oxydoréduction, il faut premièrement écrire les demi-équations électroniques de chacun des couples impliqués.
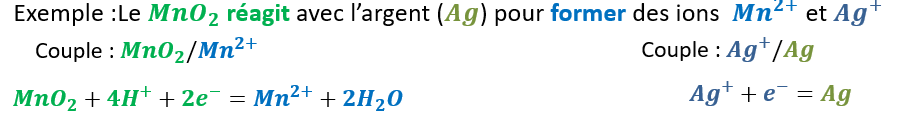
Chacune des demi-équations doit impérativement échanger le même nombre d’électrons, ce qui peut nécessiter de multiplier une demi équation par un nombre enier.
Par la suite on peut écrire les demi équations l’une au dessus de l’autre en mettant les réactifs à gauche et les produits à droite.
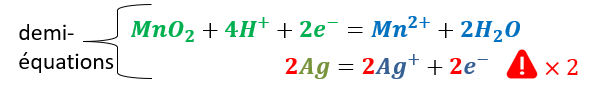
Il faut ensuite faire la somme de tous les réactifs d’une part et la somme de tous les produits d’autre part.
Pour l’équation bilan, une flêche sera utilisée pour signifier le sens de la réaction, des réactifs, vers les produits.
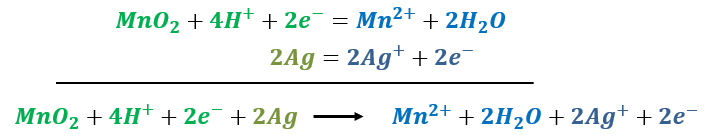
Enfin, les électrons qui sont forcément au même nombre de part et d’autre de la flêche de transformation ne doivent pas apparaître dans l’équation bilan qui s’écrira finalement:
Au vu des demi-équations des couples participants à la transformation, il est parfois nécessaire de multiplier chacune d’elle par un nombre entier différent, dans le but d’obtenir le même nombre d’électrons échangés de part et d’autre.

.